用于治疗神经母细胞瘤的孤儿药获批或改善高风险儿童临床结果
AUMBiosciencesPte.Ltd.(“AUM”)是一家专注于发现和开发精准肿瘤治疗药物的全球临床阶段生物科技公司,2022年11月30日宣布美国食品药品监督管理局(FDA)授予AUM302孤儿药资格,AUM302是一种潜在的首创口服激酶抑制剂,不仅靶向PI3K,也是PIM和mTOR等关键耐药机制,用于神经母细胞瘤的治疗。

“AUM302的孤儿药资格是我们今年产品获得的第二个孤儿药资格,标志着AUM的一个重要里程碑,因为我们推进了我们的多样化的精准肿瘤治疗药物管线,旨在逆转癌症耐药性。”AUM创始人兼CEOVishalDoshi说。“AUM302有可能成为治疗神经母细胞瘤的首创多激酶抑制剂。FDA的决定强化了我们药物开发策略和临床试验设计的优势,以提供可负担、安全和有效的肿瘤治疗。”
AUM302的临床前研究表明,用PIM/PI3K/mTOR抑制补充常规化疗治疗有可能改善高风险神经母细胞瘤儿童的临床结果以及抑制癌细胞生长,并防止耐药性出现。
一、关于AUM302大环多激酶抑制剂
AUM302是一种首创的口服激酶抑制剂,合理设计为在单药治疗中独特地结合泛PIM激酶、泛PI3K和mTOR抑制。这种多靶向能力已经被改造成单个分子,具有抑制多个关键细胞内通路的能力,增加了其抑制癌细胞生长和防止耐药性出现的能力。具有强效、良好的耐受性和良好的药物特性。AUM302是一种独特的多靶点癌症治疗药物,不仅靶向PI3K,还靶向PIM、mTOR等关键耐药机制。AUM302是一种单分子治疗药物,已进行优化以抑制这些关键通路。
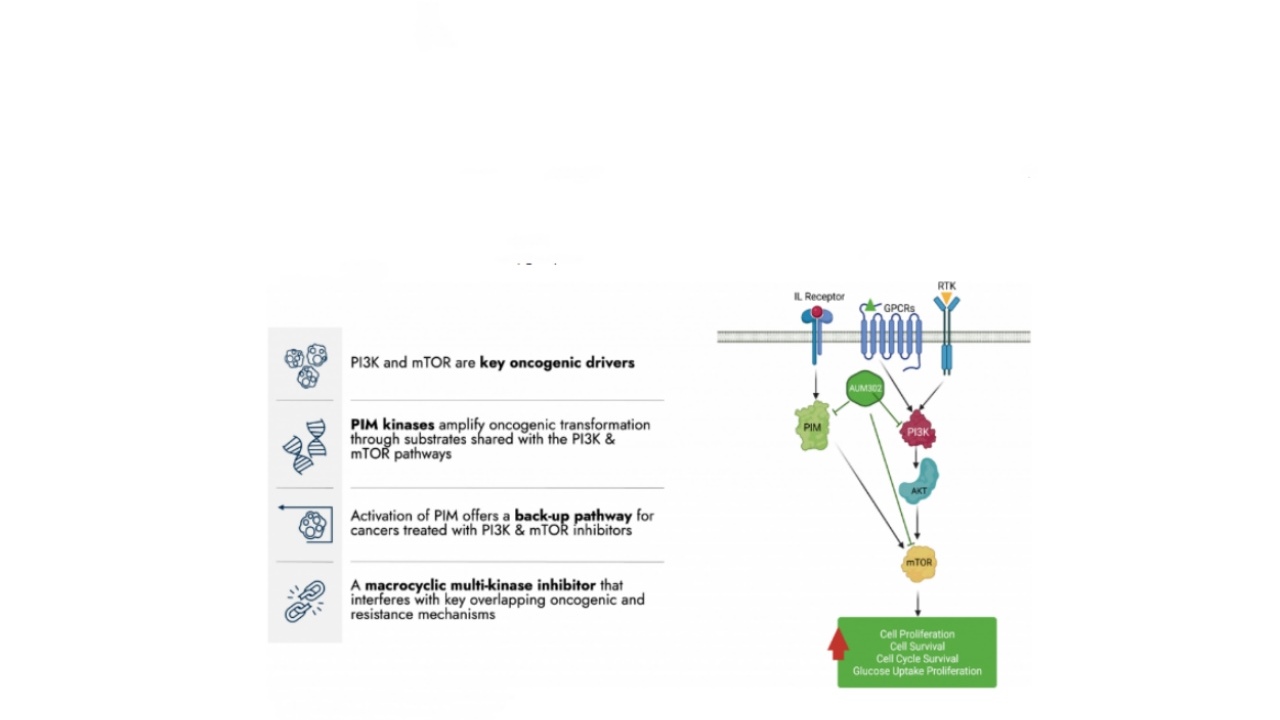
二、AUM302作用机制
PI3K/AKT/mTOR信号网络的复杂性涉及许多反馈回路、与其他信号通路和代偿通路的广泛串扰节点,为规避PI3K抑制的影响提供了充足的机会。PI3K通路的致癌性激活促进细胞生长、存活和对化疗和放疗的耐药性。关键的是,PI3K通路激活通常与其他信号网络中的促致瘤性畸变同时发生,从而使肿瘤细胞能够抵抗PI3K抑制的作用和/或容易产生这种耐药性。
FDA孤儿产品开发办公室授予预期用于治疗、诊断或预防罕见疾病的候选药物和生物制品孤儿药资格,这意味着在美国孤儿药资格认定中影响不到200,000人的疾病可提供一定获益,包括资金激励,以支持临床开发,以及如果药物最终获批用于其指定适应症,该药物在美国指定孤儿适应症的市场独占权可能长达7年。
以上文章来源于迈极康insight



