
宫腔论“见”|浙江省立同德医院宫腔疾病系列课

刘松君 妇科·主任医师
浙江省立同德医院
宫腔论“见”|浙江省立同德医院宫腔疾病系列课专题,刘松君教授进行了“子宫内膜癌诊治进展”相关授课。本次授课从以下几个方面进行:
一、分类及分子分型
1.分类
根据发病机制和生物学行为特点将子宫内膜癌分为雌激素依赖型(Ⅰ型)和非雌激素依赖型(Ⅱ型)。雌激素依赖型子宫内膜癌大部分病理类型为子宫内膜样腺癌,少部分为黏液腺癌;非雌激素依赖型子宫内膜癌病理类型包括浆液性癌、黏液性癌、透明细胞癌、癌肉瘤等。
2.分子分型
首选根据2013年癌症基因谱(TCGA),将EC重新分类。这一分型有助于提示不同肿瘤亚型的预后及选择相应的靶向治疗药物及免疫治疗。根据临床预后,EC分为4种分子亚型:POLE突变型,高度微卫星不稳定型(MSI-H),低拷贝型和高拷贝型。NCCN、FIGO、ESGO指南中均有EC分子分型推荐。
(1)分子分型检测流程
分子分型检测简化流程:最具代表性的为ProMisE分型检测,其利用MMR免疫组化替代MSI检测,P53免疫组化替代拷贝数检测。将EC分成MMR缺失(MMR-d)、POLE突变型、P53野生型(P53wt)、P53突变型(P53abn)。该分型在福尔马林固定及石蜡包埋样本中即可进行,样本要求低,便于临床收集与操作。
(2)根据ProMisE分型指导治疗
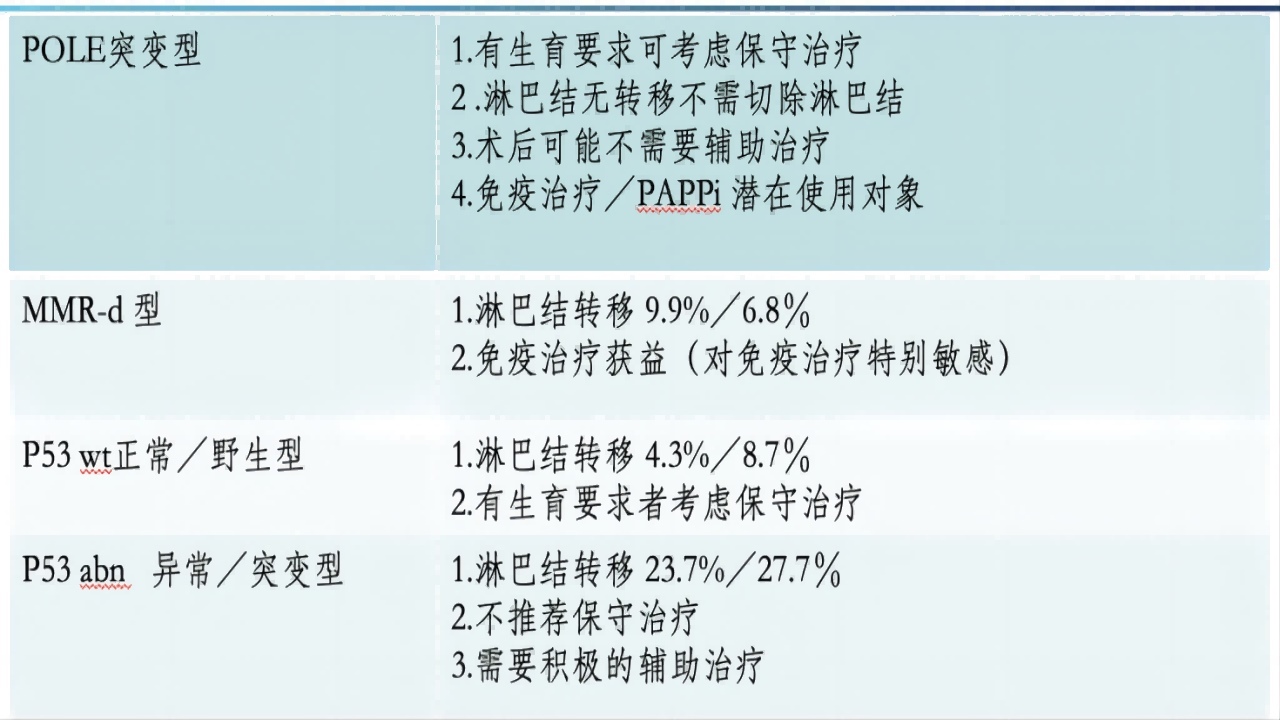
二、诊断
1.症状、体征
症状:异常阴道流血,尤其绝经后阴道出血;阴道异常流液;下腹隐痛;其他如晚期患者出现恶液质等。
体征:妇科检查早期多无异常,部分患者子宫增大变软,晚期浸及宫颈或宫骶韧带、主韧带可触及增厚。部分患者盆壁处可触及肿大淋巴结,有远处转移者,可扪及腹股沟等淋巴结。
2.辅助检查
▪超声:最常用的检测方法。
▪MRI:用来评估子宫内膜癌肿块大小以及与肌层的关系、是否累及宫颈、阴道、膀胱、直肠、盆腔内肿瘤播散、盆腔、后腹膜及腹股沟淋巴结转移情况等。
▪CT及PET-CT:适用于子宫内膜癌复发及转移性癌患者。
▪血液及肿瘤标志物:缺乏特异性的肿瘤标志物。
3.筛查方法
宫腔镜下定位活检或诊刮子宫内膜标本行病理学检查是子宫内膜癌确诊“金标准”。
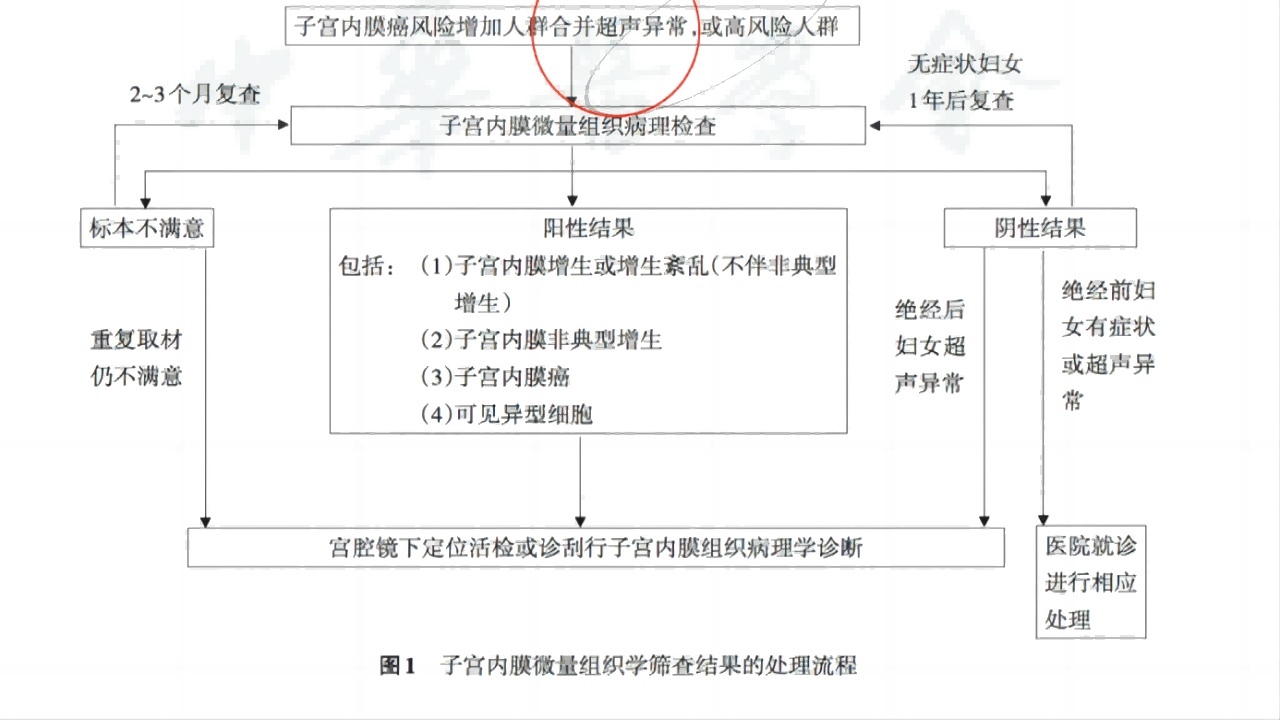
三、分期
1.2009FIGO分期

2.2023FIGO分期


四、治疗
治疗原则:以手术治疗为主,辅以放疗、化疗和激素等综合治疗。
(一)I期子宫内膜癌治疗
1.手术治疗
临床I期(子宫内膜癌局限于子宫体):
(1)首先行腹腔冲洗液或腹水细胞学检查并单独报告;
(2)术式:全子宫及双附件切除术±盆腔及腹主动脉旁淋巴结切除术;
(3)根据术后病理明确手术-病理分期及辅助治疗的应用;
(4)手术经腹、阴道或腹腔镜或机器人均可,需完整取出子宫(最基本原则),避免粉碎和分块取出子宫;
(5)小子宫首选经阴道取出,大子宫推荐经腹取出。
(6)年轻子宫内膜癌患者保留卵巢,则须符合以下条件:①年龄<45岁;②IA期;③高分化;④术前和术中评估无可疑淋巴结转移;⑤具有随访条件;⑥没有BRAC/Lynch家族史。
2.淋巴清除问题
患者合并高危因素包括深肌层浸润、高级别癌、浆液性腺癌、透明细胞癌、癌肉瘤等,需切除主动脉旁淋巴结至肾血管水平。若患者病灶较小(病灶大于2.0cm)、或仅为浅肌层浸润、或分化低(G1-2)可仅切除盆腔淋巴结。根据梅奥标准,若为病灶局限低危患者,没有增大淋巴结,侵犯小于1/2肌层,肿瘤直径小于2.0cm,且肿瘤分化低(G1和G2),建议结合分子分型来决定是否需要清扫淋巴结。
关于前哨淋巴结的利弊还值得进一步研究。前瞻性随机研究发现早期子宫内膜癌淋巴结切除的程度与生存无关。由于淋巴结切除的数目、范围以及辅助治疗方法的不同,8%—50%的子宫内膜癌淋巴清扫后患者会出现下肢淋巴水肿。因此,前哨淋巴结定位逐渐成为手术分期的一种方法。NCCN指南推荐病变局限于子宫的子宫内膜癌可考虑前哨淋巴结活检,以替代系统淋巴结切除术。
3.保留生育功能治疗
(1)需具备的条件
①经病理专家核实,病理类型为子宫内膜样腺癌,G1级。
②MRI(首选)或经阴道超声检查发现病灶局限于子宫内膜,影像学检查未发现可疑的转移病灶。
③无药物治疗或妊娠禁忌证。
④经充分解释,患者了解保留生育功能并非子宫内膜癌的标准治疗方式,并在治疗前咨询生殖专家。
⑤对合适的患者进行遗传咨询或基因检测:排除Lynch综合征和BRAC突变,分子分型为POLE突变或低拷贝型可考虑,子宫内膜样腺癌G2级、浅肌层浸润可尝试。
⑥具备随访条件。
(2)治疗
主要为药物治疗,包括甲地孕酮、醋酸甲羟孕酮和左炔诺孕酮宫内缓释系统。最常用的口服孕激素:醋酸甲羟孕酮(400~800mg/d)或醋酸甲地孕酮(160mg/d,分2或4次服用)。
治疗期间每3~6个月进行一次分段诊刮或取子宫内膜活检。若6月后病变完全缓解,鼓励患者受孕;若未受孕,孕前持续每3~6个月进行一次内膜取样检查;若患者暂无生育计划,予孕激素维持治疗和定期监测;若子宫内膜癌持续存在6~12个月,则行全子宫+双附件切除+手术分期;完成生育后或内膜取样发现疾病进展,即行全子宫+双附件切除+手术分期。
4.术后治疗
结合疾病分期、组织分化和高危因素决定,需要术后治疗者,在阴道残端愈合后尽快开始放疗,一般不超过12周。高危因素包括年龄大于60岁、LVSI(+)、深肌层浸润、中低分化。处理措施为:伴有一个高危因素者,观察或阴道后装放疗;伴有二个高危因素者,阴道后装放疗或外照射;伴有三个高危因素者,外照射±化疗(IB或G3)。
(二)Ⅱ期子宫内膜癌治疗
1.手术治疗
临床Ⅱ期(子宫内膜癌侵犯宫颈间质):
①进入盆/腹腔后首先行腹腔冲洗液细胞学检查;
②标准手术方式:全子宫双附件切除术+盆腔及腹主动脉旁淋巴结切除术;根治性子宫切除仅用于需要达到阴性手术切缘时;
③根据术后病理明确手术-病理分期及辅助治疗的应用;
④不能手术者外照射+阴道近距离放疗±化疗再重新评估是否可以手术。
2.术后治疗
首选外照射放疗和/或阴道近距离放疗±化疗(2B级证据);广泛全子宫切除术后切缘阴性也可以观察;G1或G2、肌层浸润小于50%,LVSI阴性,宫颈微小浸润者,术后也可选择补充阴道近距离放疗。
(三)早期子宫内膜癌手术治疗注意事项
分期手术中需行全面探查,评估腹膜、膈肌及浆膜层有无病灶,在任何可疑部位取活检以排除子宫外病变;推荐入腹后取腹水/腹腔冲洗液细胞学检查并单独报告;电凝或钳夹双侧子宫角处输卵管峡部,避免术中操作造成宫腔内肿瘤循输卵管扩散至盆腔;切除子宫后剖视子宫检查,必要时行冰冻切片病理检查。手术记录应明确癌瘤大小、部位(宫底部或子宫下段/宫颈)、肌层浸润深度(占整个肌层的比例)、宫颈峡部及双侧附件有无受累等。
(四)Ⅲ-Ⅳ期子宫内膜癌治疗
1.手术治疗
临床Ⅲ期及以上的EC以综合治疗为主。建议行包括子宫+双附件切除在内的肿瘤细胞减灭术。手术目标是RO切除;也可考虑新辅助化疗后再手术。病变超出子宫但局限在盆腔内(转移至阴道、膀胱、肠/直肠、宫旁、淋巴结)无法手术切除者,可行外照射放疗和/或阴道近距离放疗±全身治疗,也可单纯化疗后再次评估是否可以手术治疗,或者根据治疗效果选择放疗。病变超出腹腔或转移到肝脏者,可行化疗和/或外照射放疗和/或激素治疗,也可考虑姑息性子宫+双附件切除术。
2.术后处理
临床Ⅲ期及以上的EC术后可行化疗±外照射放疗±阴道近距离放疗,推荐联合治疗而不是序贯治疗;ⅢC期者首选化疗联合放疗。
(五)高危组织类型子宫内膜癌的治疗
1.手术治疗
Ⅱ型子宫内膜癌包括浆液性腺癌、透明细胞癌和癌肉瘤,其治疗遵循卵巢癌的手术原则和方式,除包括腹水细胞学检查、全子宫双附件切除术及盆腔淋巴结和腹主动脉旁淋巴结切除术外,还应行大网膜切除术及腹膜多点活检。如为晚期,则行肿瘤细胞减灭术。
2.术后辅助治疗
ⅠA期:首选化疗+阴道近距离放疗或外照射放疗。
ⅠB-Ⅳ期:化疗±外照射放疗±阴道近距离放疗。
(六)子宫内膜癌全身化疗
全身化疗主要用于晚期(Ⅲ~Ⅳ期)或复发患者以及特殊病理类型患者,方案推荐为紫杉醇+卡铂;其他常用方案如多西他赛联合卡铂、多柔比星联合顺铂、脂质体多柔比星等。对于晚期患者,ⅢA~ⅢC期推荐的方案为全身化疗和/或体外放疗±腔内放疗,ⅣA/ⅣB期主要治疗为全身化疗。
(七)子宫内膜癌激素治疗
激素治疗仅用于子宫内膜样腺癌,主要为孕激素,用于早期子宫内膜癌需保留生育功能的年轻患者及晚期、复发性或无法手术的患者。以高效药物、大剂量、长疗程为佳,4-6周显效。最常用的孕激素主要有3种:醋酸甲羟孕酮(MPA),500-1000mg/d,口服;醋酸甲地孕酮(MA),160mg/d,口服;左炔诺孕酮宫内装置。其他药物包括他莫昔芬、芳香化酶抑制剂等。目前不推荐早期患者术后常规应用激素治疗。
(八)新型靶向治疗及免疫治疗
随着对肿瘤分子机制研究的深入,子宫内膜癌的靶向治疗、免疫治疗也逐渐成为研究的热点。
曲妥珠单抗:对于Ⅲ/Ⅳ期和复发的子宫内膜浆液性癌,且HER2表达阳性患者,可在TC方案上加用曲妥珠单抗。
MMR缺陷型子宫内膜癌中常见磷酸酰肌醇3激酶(PI3K)/蛋白激酶B(Akr)哺乳动物雷帕霉素靶蛋白(mTOR)信号通路的激活,该信号通路的抑制剂是近年来子宫内膜癌靶向治疗研究的热点之一。PARPi等在体外实验中对MMR缺陷型肿瘤有良好的抑制作用。
MMR缺陷型子宫内膜癌的免疫检查点阻断治疗,2017年(FDA)已批准PD-L1抑制剂——派姆单抗用于治疗各种MSI肿瘤。
贝伐珠单抗是一种针对VEGF的单克隆抗体,作为复发子宫内膜癌治疗药物之一。
五、复发及转移的临床处理
对于初次只是接受手术的局部区域复发患者,首选的初步治疗应为放疗联合VBT,考虑在挽救性放疗中增加全身治疗。
对于放疗后复发性疾病患者,只有在预期能完全减瘤且发病率可接受的情况下,才考虑手术。可考虑术后补充全身治疗。一线标准化疗是卡铂AUC5-6加紫杉醇175mg/m2,每21天一次,共6个周期。二线化疗没有标准方案,多柔比星和紫杉醇周疗被认为是最具活性的疗法。
激素治疗可考虑作为低级别子官内膜样组织学癌患者的一线系统治疗,主要为孕激素,醋酸甲羟孕酮200mg和醋酸甲地孕酮160mg是推荐的药物。
在MSI-H/dMMR子宫内膜癌患者铂类治疗失败后,可考虑免疫验查点(ICB)单药治疗。多塔利单抗最近已被EMA和FDA批准用于此适应症。派姆单抗被FDA批准用于治疗TMB-H实体瘤,这些肿瘤在子宫内膜癌先前治疗后进展。派姆单抗-乐伐替尼被EMA批准用于既往铂基化疗失败的子宫内膜癌患者,不适合接受治愈性手术或RT患者,FDA批准适用于非dMMR/MSI-H的子宫内膜癌患者。
[声明:本网站所有内容,凡未注明来源为“转载”,版权均归巢内网所有,未经授权,任何媒体、网站或个人不得转载,否则将追究法律责任,授权转载时须注明“来源:巢内网”。本网注明来源为其他媒体的内容为转载,转载仅作观点分享,版权归原作者所有,如有侵犯版权,请及时联系我们]
精彩回放

子宫动静瘘诊治及病例分享
宫腔论“见”|浙江省立同德医院宫腔疾病系列课专题,刘松君教授进行了“子宫动静瘘诊治及病例分享”相关授课。本次授课从以下几个方面进行:一、概况二、病因;三、临床特征;四、诊断;五、鉴别;六、治疗;七、子宫动静脉瘘病例分享;八、总结;等。
